近期干细胞研究进展汇总!
1.Science:激活溶酶体可让衰老的神经干细胞恢复青春
在一项新的研究中,来自美国斯坦福大学医学院的研究人员发现在小鼠大脑中,年轻的静止性神经干细胞(resting neural stem cell)在它们的溶酶体(细胞中的一种特定的细胞器,用于处理细胞垃圾)中储存着大量的蛋白聚集物。相 关研究结果发表在2018年3月16日的Science期刊上,论文标题为“Lysosome activation clears aggregates and enhances quiescent neural stem cell activation during aging”。论文通信作者为斯坦福大学老化生物学中心副主任Anne Brunet,论文第一作者为博 士后研究员Dena Leeman博士。 这些研究人员先是观察静止性神经干细胞的基因表达谱与那些对触发新的神经元产生的外部信号作出反应的活化神经干细胞(activated neural stem cell)的基因表达谱之间可能存在的差异。他们比较了当它们衰老时,它们如何作出改变。
Leeman从来自年轻小鼠和老年小鼠的大脑中分离出几种细胞群体进行研究,包括静止性神经干细胞、活化神经干细胞和由活化神经干细胞产生的神经祖细胞。她发现静止性神经干细胞表达许多与溶酶体相关的基因,而活化神经干细胞表达与一种参与蛋白破坏的蛋白复合 物(被称作蛋白酶体)相关的基因。严格控制蛋白产生和清除可让细胞维持必需的蛋白库存来以执行所需的细胞功能。
当Leeman利用一种结合到蛋白聚集物上的染料对年轻的静止性神经干细胞和活化神经干细胞进行染色时,她吃惊地发现静止性神经干细胞经染色后变得更加明亮,不过它们具有较低的蛋白产生率。Leeman还发现,相比于活化神经干细胞,年轻的静止性神经干细胞在它们 的溶酶体中相对较慢地堆积这些蛋白聚集物。
2.JCI:上海交大医学院发现清除白血病干细胞的潜在新靶点
白血病干细胞是与白血病发生、发展和复发有关的一群细胞,在白血病干细胞上发现新的治疗靶点对于彻底治愈白血病有至关重要的意义。最近来自上海交通大学医学院的郑俊克和陈国强院士等人在白血病干细胞上发现了一个高表达的基因,并揭示了该基因参与白血病发生的重要机制。相关研究结果发表在国际学术期刊JCI上。
在这篇报道中,研究人员发现JAM3(junctional adhesion molecular 3)在小鼠和人的白血病干细胞中高水平表达,在MLL-AF9诱导的小鼠急性髓系白血病模型的系列移植过程中清除Jam3能够几乎完全阻止白血病的发生过程。相比之下,jam3缺失并不会影响小鼠造血干细胞的功能。
除此之外,研究人员还发现敲低JAM3会导致人白血病细胞系和原代白血病干细胞的增殖受到抑制。机制研究表明JAM3能够直接与LRP5发生相互作用激活下游的PDK1/AKT信号途径,随后GSK3β发生下调,β-catenin/CCND1信号途径发生激活,以维持白血病干细胞的自我更新能力和进入细胞周期的能力。
3.Science:揭示动物组织再生蓝图
在一项新的研究中,来自美国怀特海德研究所的研究人员描述了一种关于真涡虫(planarian)眼睛再生的模型:真涡虫的眼睛再生受到同时发挥作用的三个原则的调控,这有助了解真涡虫的祖细胞如何在再生中发挥功能。这种模型涉及位置线索;吸引祖细胞到现存结构的自组织(self-organization);起源自分散的空间区域而不是起源自精确位置的祖细胞,从而给它们的迁移路径提供灵活性。这三个原则似乎确定着祖细胞在再生期间如何决定迁移到何处进行形态和功能重建,并且它们让我们从系统水平上理解这个过程更接近一步。相关研究结果于2018年3月15日在线发表在Science期刊上,论文标题为“Self-organization and progenitor targeting generate stable patterns in planarian regeneration”。论文通信作者为怀特海德研究所研究院、麻省理工学院生物学教授和霍华德休斯医学研究所研究员Peter Reddien博士。
Reddien和他的实验室花了十多年的时间利用一种被称作真涡虫的小扁虫来揭示再生之谜。如果一个真涡虫的头部被截断,或者它的一侧被切除,那么它的每一部分(比如它的被截断的头部和剩余的部分)都会再生出整个动物。为了理解祖细胞在动物再生的嘈杂环境中如何决定迁移到哪里,这些研究人员使用了真涡虫的眼睛,它是一个肉眼看得见的器官,该器官足够小以至于可在不会产生严重损伤的情况下将它切除,此外,它还含有人们已确定的祖细胞分子标志物。
这些研究人员设计了一个简单的实验来解决这些祖细胞如何决定迁移到哪里的问题:截断真涡虫的头部,接着在三天后从这个被截断的头部部分移除一只眼睛。他们发现祖细胞会在位于剩余的一只眼睛的前面开始形成一只新的眼睛,而不是在解剖结构确定的“正确”位置(与剩余的这只眼睛相对称的位置)上形成一只新的眼睛。但是,如果在更早的时候---与头部截断的同一天而不是在三天后---从被截断的头部部分移除一只眼睛,然后开展相同的实验,那么会产生不同的结果:新的眼睛在与剩下的一只眼睛相对称的位置---也就是身体结构的“正确”位置---上开始形成,这提示着当多种选择存在冲突时,解剖结构的自组装动力学取胜。
这些简单的规则指导这种动物成功再生,并且当它的再生潜能被最大限度地挖掘时会产生替代性的稳定的解剖结构形态:产生具有三只眼睛、四只眼睛或五只眼睛的真涡虫。切除这种动物的一侧并且截断它的头部能够让它的祖细胞足够远地远离现有的眼睛,从而允许在头部部分中开始形成第三只眼睛。
4.Nat Biotechnol:干细胞疗法治疗黄斑退化
2015年6月, 86岁的Douglas Waters出现了严重的老年性黄斑变性症状(AMD),导致难以看清东西。几个月之后,他成为了UC Santa Barbara的研究者开发的利用干细胞诱导分化的视觉细胞治疗AMD的临床试验的一员。在手术之前,Douglas的视力很差,右眼几乎看不到任何东西。而手术之后,他的视力恢复地很快,能够阅读报纸以及干一些农活。这项出色的临床治疗结果发表在最近一期的《Nature Biotechnology》杂志上,该文章描述了将从干细胞诱导而来的,工程化的视网膜色素上皮细胞移植进入患者的眼睛中,从而帮助AMD患者重建光明。结果表明该方法具有安全性以及有效性。
黄斑变性是发达国家中造成50岁以上人群视力损伤的主要原因。该疾病的发生主要是由于血管病变导致血液难以进入视网膜的中心黄斑区域。在这项研究中,作者希望能够使用干细胞将患者眼部后侧受损的细胞置换,从而恢复患者的视力。该手术总共耗时大概1到2小时。除了Douglas之外,该试验中还有一名60岁的女性患者。在手术后的12个月内,她与Douglas两人的视力恢复水平都十分显著。此前他们都几乎无法阅读,而手术之后则能够在佩戴正常眼镜的情况下每分钟阅读60-80个字。
5.干细胞疗法能够修复更年期的过早出现以及生育问题
新闻来源:Stem cell therapy may help reverse effects of premature menopause, restore fertility
最近一项临床研究指出,通过自体骨髓移植的手段能够使因卵巢功能早衰而生育力下降的女性重新恢复生育能力,而且避免过早地进入更年期。相关结果在最近于芝加哥召开的第100届内分泌学会年度会议上得到了展示。
"在接受治疗的两名受体中,我们发现其血清雌激素水平在接受干细胞移植后的三个月后出现了明显升高,而且该效应能够持续一年之久。患者的更年期症状得到了缓解。干细胞移植六个月后其经期得到了重新恢复"。该研究的高级作者,来自伊利诺伊斯大学的教授Ayman Al-Hendy说道。
研究者们计划招募33名参与者进行临床试验,在目前已经接受治疗的两名患者中,他们从每名患者的髂嵴处提取了间叶干细胞并且通过微创腹腔镜的手段将细胞注入自身一侧卵巢中,同时保证另外一侧卵巢不受影响。之后,研究者们定期对患者的血常规、卵巢成像以及更年期症状进行调查。
由于研究者们发现接受治疗的女性其雌激素水平有明显上升,而且开始出现经期反应。因此,研究者们希望能够进一步恢复患者的生育能力。
6.Nat Med:首次证实人神经干细胞移植可改善脊髓损伤猴子的抓力
在一项新的研究中,研究人员报道移植到猴子受损脊髓中的人神经干细胞成熟为神经元,触发神经连接形成,从而让这些猴子抓住橙子的能力得到改善。相关研究结果近期发表在Nature Medicine期刊上,论文标题为“Restorative effects of human neural stem cell grafts on the primate spinal cord”。
在这项研究中,Tuszynski和他的同事们切掉猕猴的一段脊髓,然后在两周后将人神经祖细胞(neural progenitor cell)移植到这种脊髓损伤部位。在首批4只猴子中,这些细胞移植物没有保持在原位,这一发现迫使这些研究人员将更多的纤维蛋白原-凝血酶(fibrinogen–thrombin)添加到这些细胞移植物中。纤维蛋白原-凝血酶是一种蛋白-酶混合物,可让这些移植物更快地附着到损伤位点上。Tuszynski团队还不得不让手术台倾斜以便排出脑脊液,这是因为脑脊液会将这些移植物冲走。
经过这些调整后,在剩余的5只猴子中,这些移植的神经干细胞保留在原位,而且这些研究人员观察到这些移植的干细胞发育成神经元和神经胶质细胞。在损伤部位中,这些人神经元产生高达15万个线状轴突,这些轴突从移植位点处向外延伸高达50毫米,并且早在这些新产生的神经细胞就位两个月后,这些研究人员就能够观察到它们与猴子本身的神经细胞建立神经连接。在大多数情况下,细胞移植物附着在脊髓损伤部位的猴子能够更好地操纵它们的手指,使它们的手指绕着橙子弯曲,而细胞移植物未附着的猴子并不能握住橙子,它们的手指保持折叠,因此橙子停留在它们的指关节上。
7.Nature:揭示SMAD2/3协调人多能性干细胞发育
为了让细胞和组织正常地发挥功能,某些基因需要在正确的时间开启和关闭,以响应来自细胞外的生长因子信号。已知SMAD2和SMAD3(SMAD2/3)蛋白是这个细胞信号转导过程的一个重要的组成部分,在细胞内部被激活,开启和关闭许多不同过程(从胚胎发育和生长到激活免疫系统或癌症)所需的基因。
在一项新的研究中,来自英国剑桥大学的研究人员研究了人多能性干细胞---能够产生人体所有组织和器官的细胞---中的SMAD2/3与其他蛋白之间的相互作用。他们发现尽管SMAD2/3确实结合一些转录因子,但是它们也与参与细胞中的一系列分子过程的蛋白发生相互作用,从而协调这些蛋白进行细胞信号转导。相关研究结果发表在2018年3月8日的Nature期刊上,论文标题为“The SMAD2/3 interactome reveals that TGFβ controls m6A mRNA methylation in pluripotency”。
这些研究人员首次观察到SMAD2/3能够激活经过RNA编辑的蛋白,从而使得特定的mRNA变得不稳定和快速地降解。SMAD2/3发挥的作用是将细胞信号转导与RNA编辑相关联在一起,从而允许细胞开启和随后再次关闭对发育至关重要的基因。鉴于SMAD2/3的活性受到生长因子的调节,这项研究阐明了胞外信号能够控制细胞功能的一种新方式。
8.Nat Protocol:科学家们培育出人类心脏3D模型

心脏是胚胎期第一个发育的器官,同时也是引发家长们顾虑的第一个器官。对于准妈妈们来说,怀孕的喜悦往往会被接受医生检查的不安感所掩盖。家长们与医生们往往要考虑母亲的健康以及接受药物治疗后会对胎儿可能产生的影响。美国FDA要求所有药物必须注明对孕妇以及婴儿可能产生的威胁。一些药物标签上注明了其在动物水平的检测中没有发现致病风险,但还没有在孕妇群体中进行仔细的研究。
Ma等人一直致力于研究人源诱导多能性干细胞(ips)技术在组织再生以及干细胞工程方面的应用。“这类干细胞能够分化形成机体的任何类型的细胞”。多能性干细胞能够再生形成心脏组织,但Ma等人相信他们能够走得更进一步。
作者等人基于生物材料以及干细胞技术,建立了心脏的3D组织模型,该模型能够模拟人类心脏的早期发育阶段。通过在组织培养皿中加入一层多聚物,以及在其表面蚀刻形成微小的痕迹。范细胞能够与上述痕迹牢固地结合。由于干细胞本身并不会粘附在多聚物上,因此他们能够沿着蚀刻痕迹生长,并最终发育形成3D结构。作者等人的研究重点在于心脏组织,但其它实验室也可以利用上述技术建立其它组织以及器官。相关结果发表在最近一期的《Nature Protocol》杂志上。
9.Sci Transl Med:重磅!利用牙龈中的间充质干细胞来加速伤口愈合!
我们常常会注意到口腔内的伤口愈合速度会比其它部位的伤口愈合速度要快,牙龈组织的修复速度大约是皮肤损伤修复速度的两倍,而且其还能减少疤痕的形成,其中一个原因或许就是牙龈间充质干细胞(gingival mesenchymal stem cells,GMSCs),其能够产生多种类型的细胞;近日,一项刊登于国际杂志Science Translational Medicine上的研究报告中,来自宾夕法尼亚大学的科学家就通过研究阐明了牙龈间充质干细胞加速组织修复的新型分子机制。
早期研究中,研究人员发现,间充质干细胞能够通过在胞外囊泡中释放信号分子来发挥多种功能,因此,理解如何有效区分牙龈组织和皮肤组织中间充质干细胞非常重要,这项研究中,研究人员对来自牙龈和皮肤中的间充质干细胞的功能进行了对比,他们发现,GMSCs包含多种蛋白质,包括炎症抑制因子IL-1RA,其能够阻断促炎性细胞因子的释放,同时IL-1RA还能被用作治疗风湿性关节炎的新型疗法。
随后研究人员重点寻找了到底是什么能够控制IL-1RA和其它细胞因子的释放,研究者推测这或许是Fas蛋白诱发的,因为该蛋白与机体的免疫调节存在一定关联;相比皮肤中的间充质干细胞而言,牙龈中的间充质干细胞含有更多的Fas蛋白,而且缺失Fas的小鼠机体中IL-1RA的水平也较低,其所释放的物质水平也会下降。随后的分子探针研究结果表明,Fas能够形成Fap-1和Cav-1的蛋白复合体来诱发小型胞外囊泡的释放,为了鉴别出这与伤口愈合的关联,研究人员对伤口组织进行了检测,他们发现,IL-1RA在伤口周围的GMSCs中水平会增加,而缺失IL-1RA的小鼠的牙龈愈合速度也会明显减慢。
相比较而言,当研究人员从GMSCs分离IL-1RA后,并将其注射到创伤部位时,明显加速了伤口的愈合速度。研究者Kou说道,我们发现,间充质干细胞,尤其是牙龈中的间充质干细胞能够通过胞外囊泡释放大量的细胞因子;相关研究发现或许对于糖尿病患者具有明显的治疗意义,研究者指出,相比健康小鼠的GMSCs而言,糖尿病小鼠机体中GMSCs或许并不太会分泌胞外囊泡,而且其GMSCs中也存在较低水平的IL-1RA分泌,引入健康小鼠机体中GMSCs所释放的胞外囊泡就能够降低糖尿病小鼠的愈合时间。
10.Glia:神经干细胞再生的机制
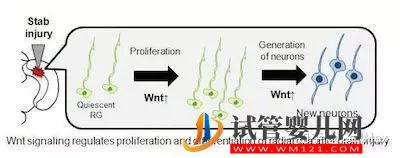
最近,来自Waseda大学的研究者们以成年斑马鱼为对象,通过建立视顶盖穿刺损伤模型,发现了神经干细胞再生的机制。该发现或许有助于人类中枢神经系统损伤的治疗。相关结果发表在最近一期的《GLIA》杂志上。
“与哺乳动物不同,斑马鱼拥有超强的神经元再生功能,因此在大脑受到损伤后能够快速激发脑组织再生过程。然而,它们的基因与人以及小鼠却无太大差异”。该研究的作者,来自Waseda大学分子神经学系的教授Toshio Ohshima说道:“此前有研究表明斑马鱼的神经元再生功能能够应用于小鼠,因此或许人类也拥有相似的潜力”。
在正常情况下,大部分放射状胶质细胞(RG)都处于静息状态,既不会增殖也不会分化。然而,当研究者们给斑马鱼的大脑进行针刺时,免疫荧光检测结果则表明RG发生分化现象,而且在第三天达到了高峰。到第七天时,受损的斑马鱼大脑与健康斑马鱼大脑之间不再存在明显差异。进一步的免疫组化实验结果表明RG能够分化产生新生神经元,修复大脑视顶盖的损伤。“通过分子机制方面的研究,我们发现Wnt信号对于调节RG的分化与新生神经元的再生十分关键”。





